【Angew.Chem.】 12万帧超长待机!西湖大学将防晒霜成分变身“超级探针”,以16纳米精度揭秘活细胞内的20分钟舞动奇迹
✨文章标题:1,3-Dicarbonyl Rhodamines for Live-Cell Single-Molecule Super-Resolution Imaging ✉️作者:Yongdeng Zhang, Dan Yang 等 🔗链接:https://doi.org/10.1002/anie.202524603
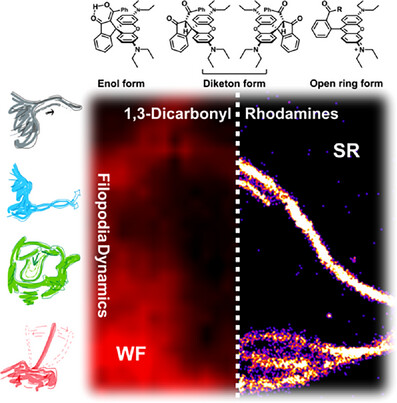
[!summary]
1. 研究背景与核心痛点
单分子定位显微术(SMLM)是超分辨成像领域的利器,能将空间分辨率提升至 5-30 纳米,远超 250 纳米的传统光学衍射极限。然而,现有的 SMLM 荧光探针面临三大挑战:
信噪比与稀疏性平衡: 成像需要分子在“开”和“关”状态间切换,且必须保持极低的瞬时分布密度(稀疏性),否则信号重叠无法定位。
光毒性问题: 传统方法往往需要极高功率的激光来诱导分子闪烁,这对活细胞是致命的。
成像时长受限: 荧光分子容易在强光下迅速漂白,难以进行长达数十分钟的动态追踪。
2. 创新设计:1,3-二羰基罗丹明(1,3-Dicarbonyl Rhodamines)
研究人员巧妙地将防晒霜成分中的常见结构——1,3-二羰基支架,整合到罗丹明荧光团中。这种设计利用了两个核心机制:
双重化学平衡: 结合了罗丹明本身的“开-关环”平衡和 1,3-二羰基的“酮-烯醇”互变异构。在这种体系下,绝大多数分子处于非荧光的“锁定”状态,天然实现了成像所需的极低发射器密度(稀疏性)。
光化学激活路径: 利用 1,3-二羰基对紫外光和单线态氧的敏感性,通过光解或光氧化反应,受控地释放出荧光发射器。
3. 关键性能指标与实验结果
高精度与高对比度: 在固定细胞成像中,实现了 16 nm 的定位精度和 105 nm 的有效空间分辨率,较宽场成像提升了约 3.3 倍。
超长时活细胞追踪: 在极低激光功率(176.7 W/cm²,远低于传统 SMLM 要求的 >500 W/cm²)下,实现了长达 20分钟、累计 120,000帧 的连续超分辨成像。
捕获细微动态: 成功捕捉到了丝状伪足(filopodia)的四种运动模式:粘附生长、缠绕生长、弯曲延伸和扫掠运动。
单激光自触发成像: 针对质膜成像,利用单线态氧介导的自催化氧化连锁反应,无需额外的 405nm 激活激光即可实现超分辨。
4. 结论与意义
该研究通过分子层面的精准设计,将“稀疏性”和“光激活”属性直接嵌入探针结构中,不仅降低了成像所需的激光能量,显著减少了对细胞的伤害,还为观察活细胞内纳米级的动态过程提供了强有力的工具。
从“痛点”到“突破”:打破纳米世界的“闪烁”枷锁
在生命科学的研究中,人类对“看见”的追求从未停止。然而,传统光学显微镜由于受到光学衍射极限的限制,其分辨率始终徘徊在 250 纳米左右,这使得科学家难以看清细胞内部细微的分子结构 。单分子定位显微术(SMLM)的出现彻底颠覆了这一现状,通过精确控制荧光分子的“开-关”状态,它能够将空间分辨率大幅提升至 5 到 30 纳米,直接触及生命活动的分子底色 。
尽管 SMLM 技术威力惊人,但在实际应用中却面临着极为严苛的挑战。传统的成像过程往往需要极高强度的激光照射,这不仅会产生巨大的光毒性,让活细胞在观察过程中迅速凋亡,还会导致荧光探针迅速发生不可逆的光漂白,使得观测时间极为短暂,往往只能捕捉到电光石火间的片段 。如何在极低的光照条件下,实现高时空分辨率且长时程的动态追踪,一直是超分辨成像领域的行业瓶颈。
针对这一核心痛点,西湖大学团队在顶级化学期刊《德国应用化学》(Angewandte Chemie International Edition)上发表了最新研究成果 。他们巧妙地从防晒霜常用成分阿伏苯宗(Avobenzone)中汲取灵感,利用 1,3-二羰基化合物独特的化学特性,成功开发出了一系列新型罗丹明荧光探针 。这种探针不仅能在极低激光功率下工作,更在活细胞成像中实现了长达 20 分钟、累计 12 万帧的超长动态观测,为细胞生物学研究提供了一把前所未有的“纳米手术刀” 。
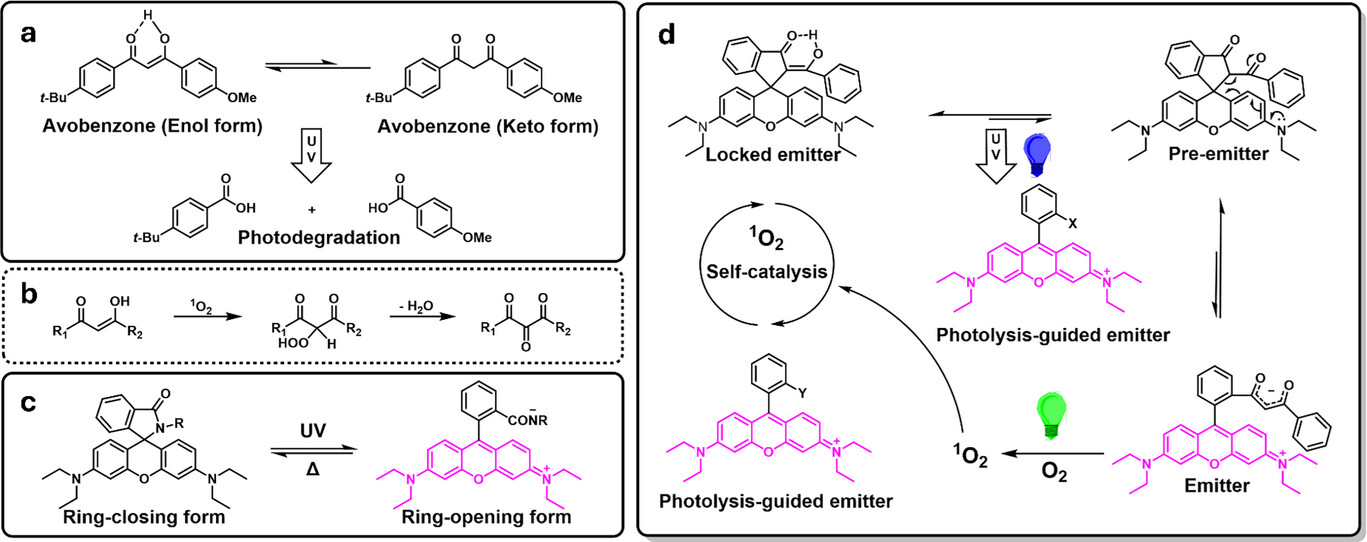
核心方法与技术细节:当防晒霜成分遇上荧光“开关”
要理解这项研究的精妙之处,首先要剖析其核心的分子设计哲学。研究团队将 1,3-二羰基骨架整合到了经典的罗丹明荧光团中 。罗丹明类探针之所以在超分辨成像中广受欢迎,是因为它们具备一种独特的“开-关环”化学平衡,即在非荧光的闭环螺旋内酯形式与具有强荧光的开环两性离子形式之间切换 。而 1,3-二羰基化合物则拥有迷人的酮-烯醇互变异构特性,这种广泛存在于医药、材料及个人护理产品中的结构,正是赋予新探针神奇功能的关键所在 。
在这种创新的双重化学平衡体系中,分子的大部分时间都处于非荧光的“锁定”状态。通过核磁共振氢谱(H NMR)的精细分析,研究者发现这种探针在溶液中主要以烯醇形式存在,其比例约为 5:1 。这种占据绝对优势的非荧光状态天然地满足了单分子定位成像对“稀疏性”的严苛要求,即在任意成像帧中,只有极少数分子被激活发光,从而避免了信号重叠造成的定位模糊 。
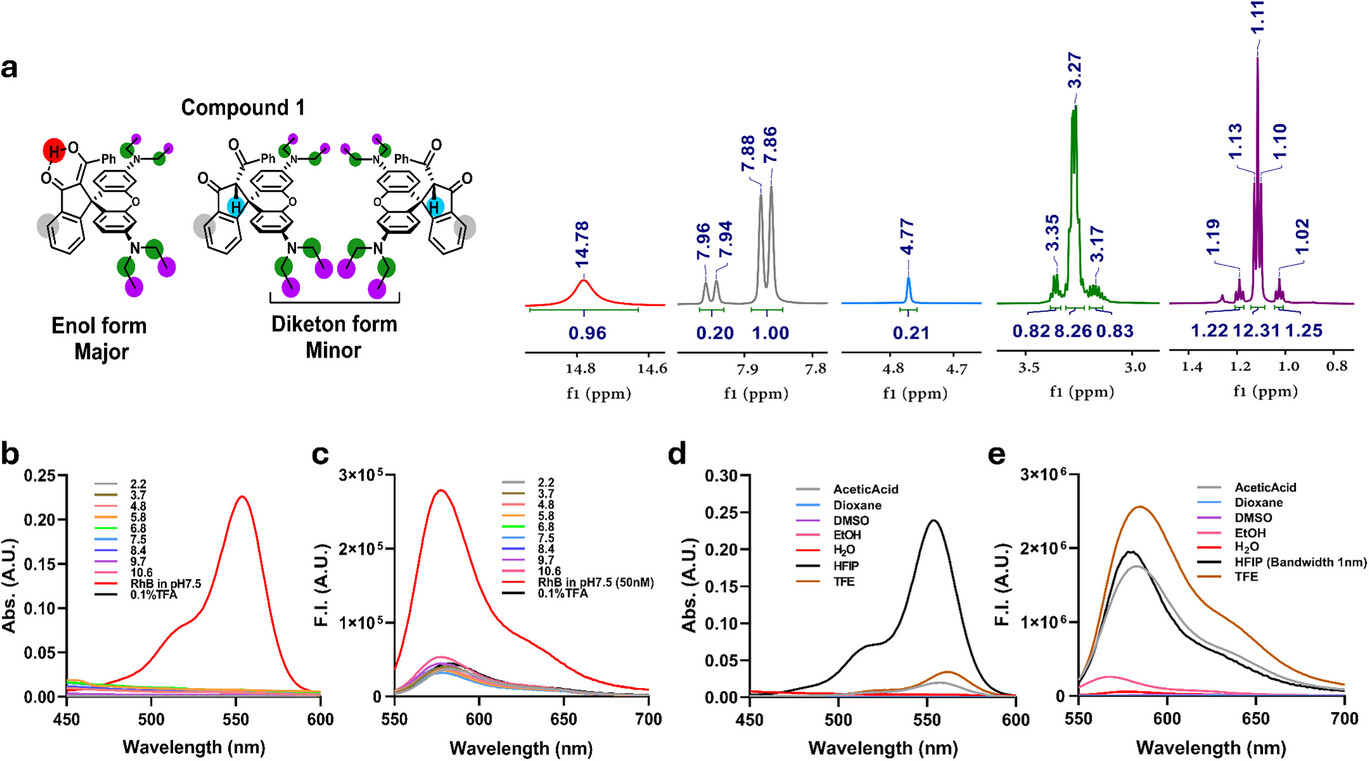
这就好比是在一个黑暗的剧场里,原本所有演员都穿着黑衣隐身在背景中。研究团队设计的 1,3-二羰基结构就像是一个智能的“暗码开关”。一小部分处于酮形式的“前发射器”可以通过环开启过程转变为发光的“发射器”,产生低密度、非重叠的信号 。更令人惊叹的是,这种探针还具备紫外光触发的光降解特性。当研究人员施加微弱的 405 纳米激光脉冲时,1,3-二羰基部分会发生光氧化断裂,释放出更多的“光解引导发射器”,从而能够根据实验需求灵活调节发射器的密度,显著提升成像的时间分辨率 。
此外,研究团队还深入探索了溶剂环境对这一双重平衡的影响。实验数据显示,在强氢键供体溶剂(如六氟异丙醇 HFIP)中,探针的吸收和荧光强度会显著增强 。这是因为溶剂分子破坏了烯醇形式的内氢键,将平衡向酮形式移动,并通过氢键作用降低了二羰基部分的电子云密度,进而促进了罗丹明核心的开环发光 。这种对电子效应和空间位阻效应的精准调控,使得研究者可以通过改变取代基(如甲氧基、电子撤回基团等),定制化地调整探针的光激活效率 。
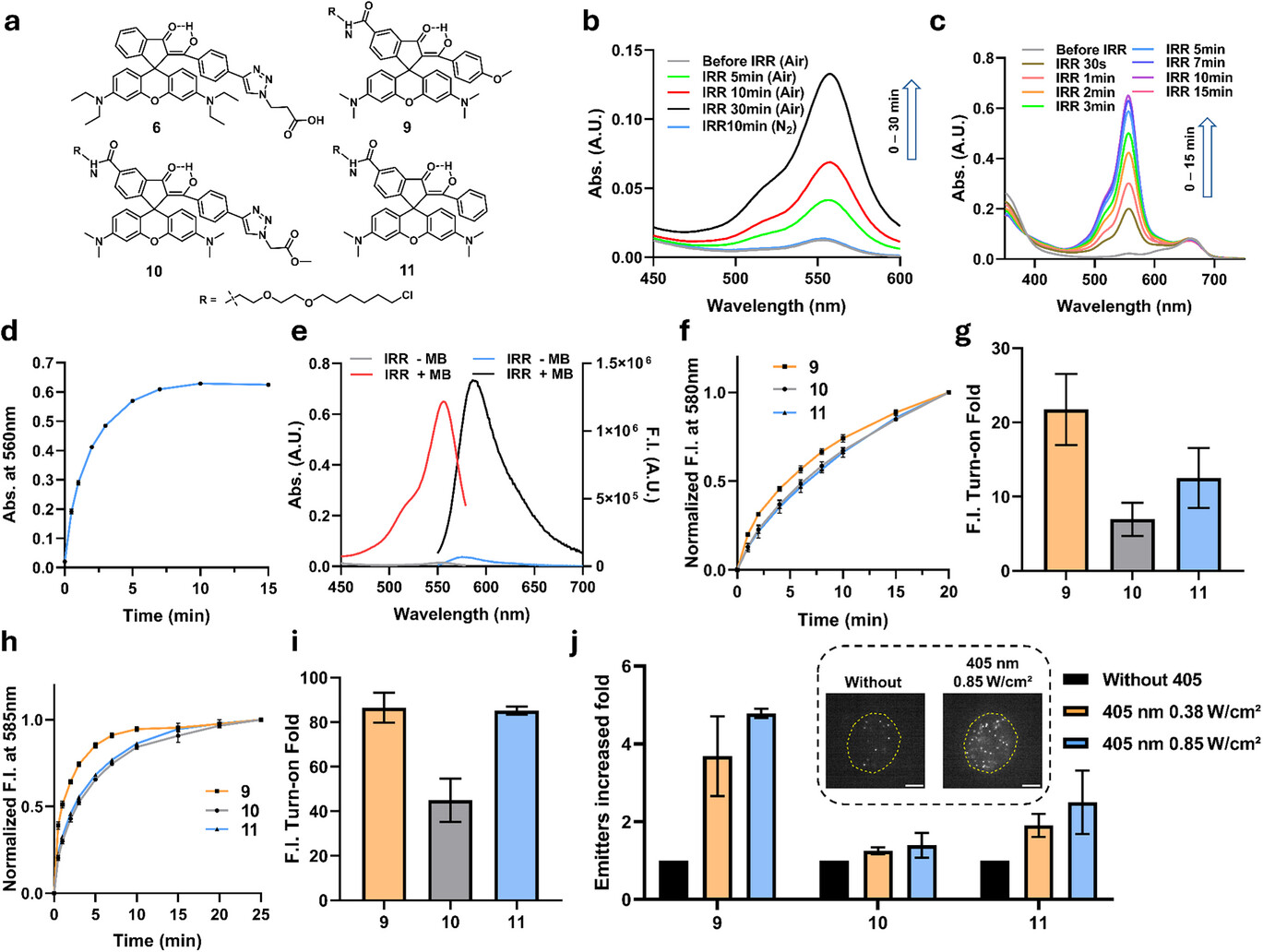
数据背后的创新与颠覆性:16纳米精度下的生命舞动
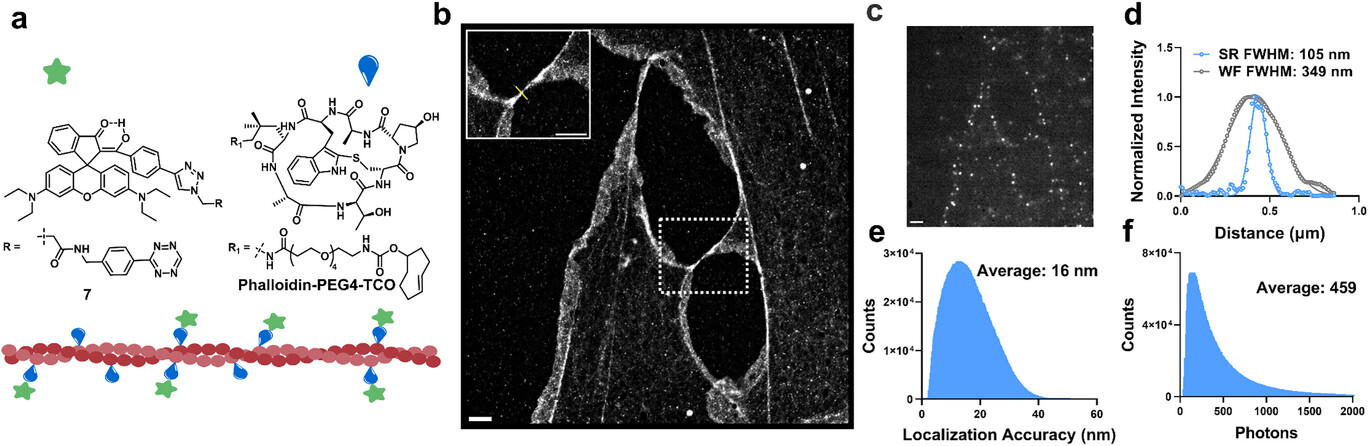
在验证了探针的化学原理后,研究团队在生物成像实验中展现了该技术近乎颠覆性的性能。首先在固定细胞成像测试中,利用点击化学方法标记的肌动蛋白(F-actin)呈现出了极高的清晰度 。实验测得其定位精度达到了惊人的 16 纳米,平均单分子光子数为 459 个 。通过重建后的超分辨图像,肌动蛋白纤维的有效空间分辨率达到 105 纳米,相比于传统宽场显微镜提升了约 3.3 倍 。
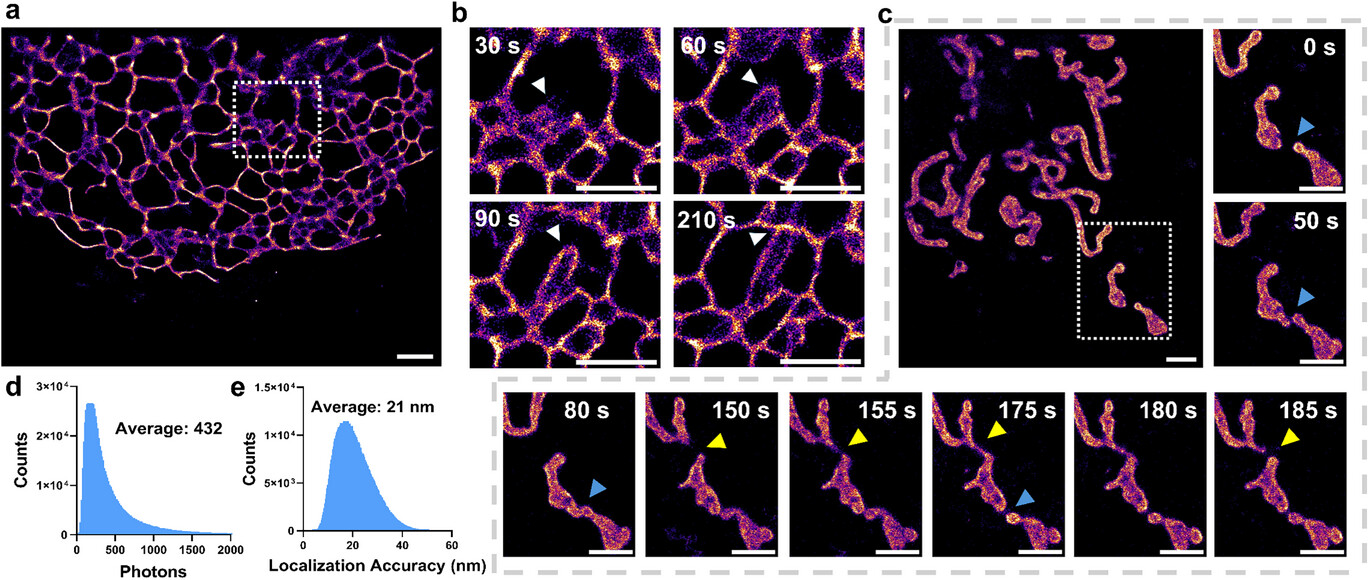
然而,真正的“重头戏”在于活细胞的长时程成像。传统 SMLM 成像往往需要高于 500 的激光功率,而西湖大学团队开发的这套系统,仅需 101.4 的极低激发激光和 0.21 的激活激光即可工作 。在这种近乎“温柔”的光照下,细胞内的内质网(ER)和线粒体动态过程被完美捕捉 。观察记录显示,内质网的连续重构、线粒体的融合与分裂等细微动作,在纳米级尺度下清晰可见,且细胞在整个成像过程中保持了极佳的生理状态 。
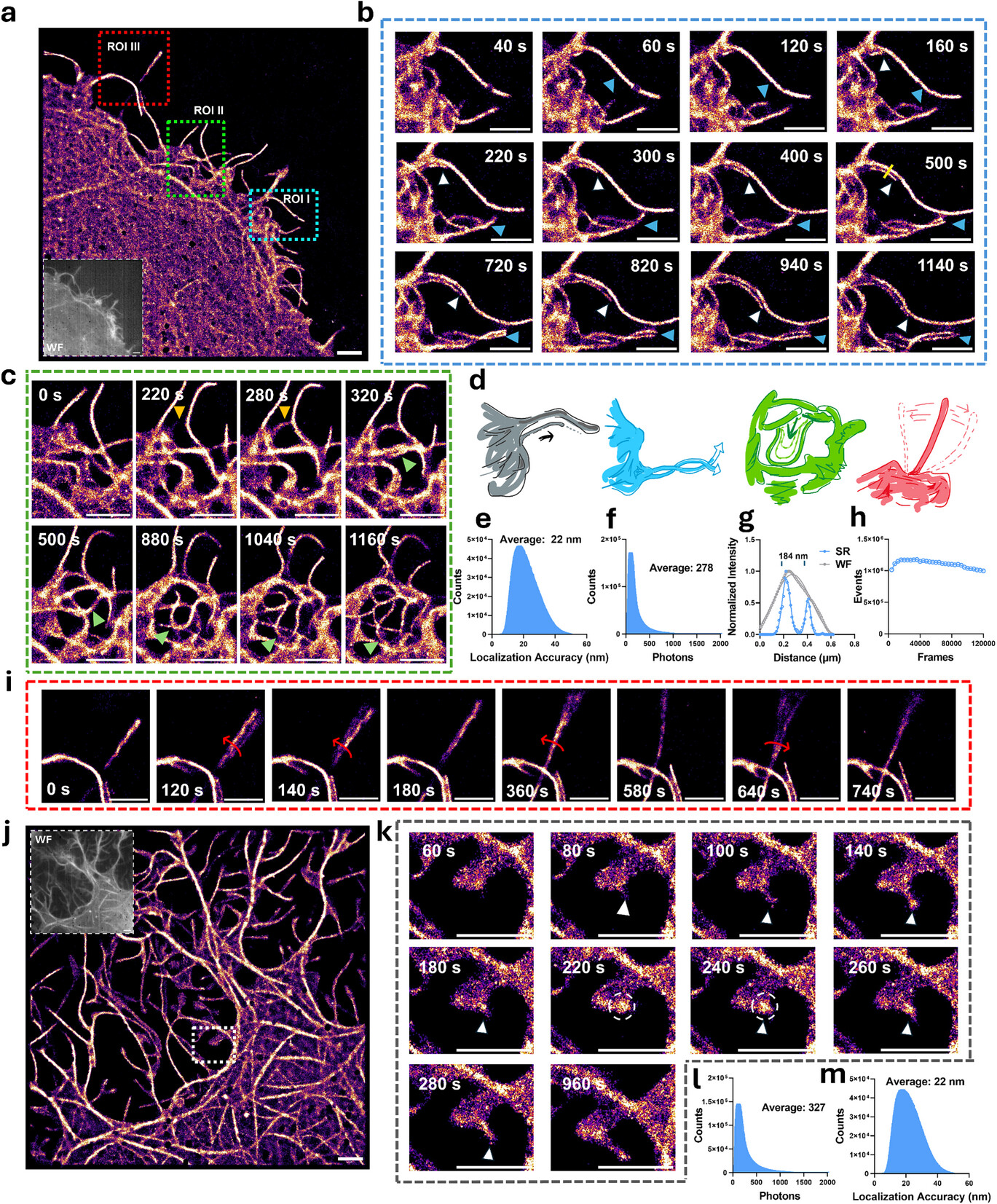
尤为令人振奋的是对丝状伪足(Filopodia)的动态追踪。丝状伪足是细胞边缘形成的细长指状突起,直径仅为 100 到 300 纳米,且其组装与拆解速度极快,通常在数秒内完成,传统成像手段极难看清其真面目 。研究人员利用 1,3-二羰基罗丹明探针,在长达 20 分钟的连续采集中,以 20 秒的时间分辨率和 22 纳米的空间精度,完整记录了丝状伪足的四种运动模式,包括粘附生长、缠绕生长、弯曲延伸以及扫掠运动 。
这组长达 12 万帧的实验数据直接证明了探针的卓越稳定性 。在 20 分钟的观测结束时,有效定位点的数量并未出现显著下降,这表明该探针具有极强的抗光漂白能力 。通过对局部定位点密度的量化分析,研究者甚至观察到了在丝状伪足延伸前,肌动蛋白在生长点的剧烈累积过程 。这种从定性观察到定量分析的跨越,为揭秘细胞感知外部环境、细胞迁移及神经发育等关键生命过程提供了全新的视角。
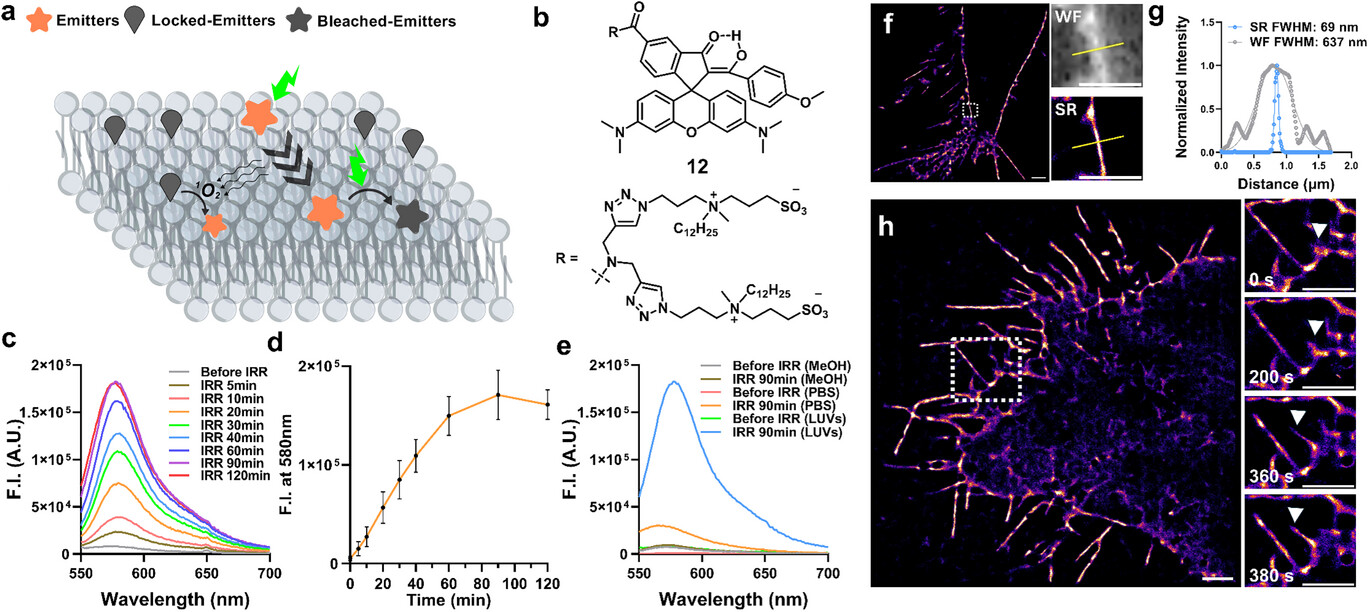
除了依赖外源光激活,研究团队还开发出了一种更具颠覆性的“自触发光氧化连锁反应”机制,专门用于细胞质膜的成像 。质膜是一个高度流动的脂质双分子层,探针分子可以在膜平面内自由扩散 。在这种特殊的微环境下,一部分发光的探针在受到激光激发时会产生单线态氧,这些活性氧分子会迅速氧化附近的处于“锁定”状态的探针,触发连锁反应,不断产生新的发射器,同时已发光的分子被光漂白 。这一自催化过程巧妙地消除了对 405 纳米激活激光的需求,实现了单激光、免洗型的超分辨质膜成像,测量得到的质膜厚度从宽场下的 637 纳米精细化到了 69 纳米 。
应用展望、局限性与未来路线图:开启纳米成像新纪元
尽管 1,3-二羰基罗丹明探针展现出了卓越的性能,但研究团队在文章中也客观地指出了其潜在的局限性。例如,在光解过程中产生的降解碎片虽然被降到了最低,但在极高精度的实验中仍需考虑其对细胞内环境的微弱影响 。此外,目前该类探针主要集中在橙红光波段,未来如何通过分子工程将其光谱扩展至近红外等更深层生物成像窗口,仍是值得探索的方向。
展望未来,这项研究不仅提供了一系列高性能的荧光探针,更重要的是确立了一种全新的 SMLM 探针设计范式。即通过在小分子骨架中直接“嵌入”稀疏性、光激活能力和低光毒性等关键属性,而非仅仅依赖外部的光物理环境调控 。这种模块化的设计策略可以轻松地与 HaloTag、点击化学以及脂质靶向基团相结合,实现对细胞内各种细胞器和功能蛋白的精准标记 。
随着这一设计理念的推广,我们可以预见,更多的亚细胞动态过程将在更自然、更健康的状态下被揭开面纱。从肿瘤细胞的早期侵袭机制到神经突触的微小信号传导,这套高精度的成像工具将有望成为生物医学研究的基础设施,推动我们对生命微观奥秘的认知进入一个新的纪元 。